Produktdatenmanagement für Medizinprodukte
Reed Tech SingleSource™ für medizinische Geräte
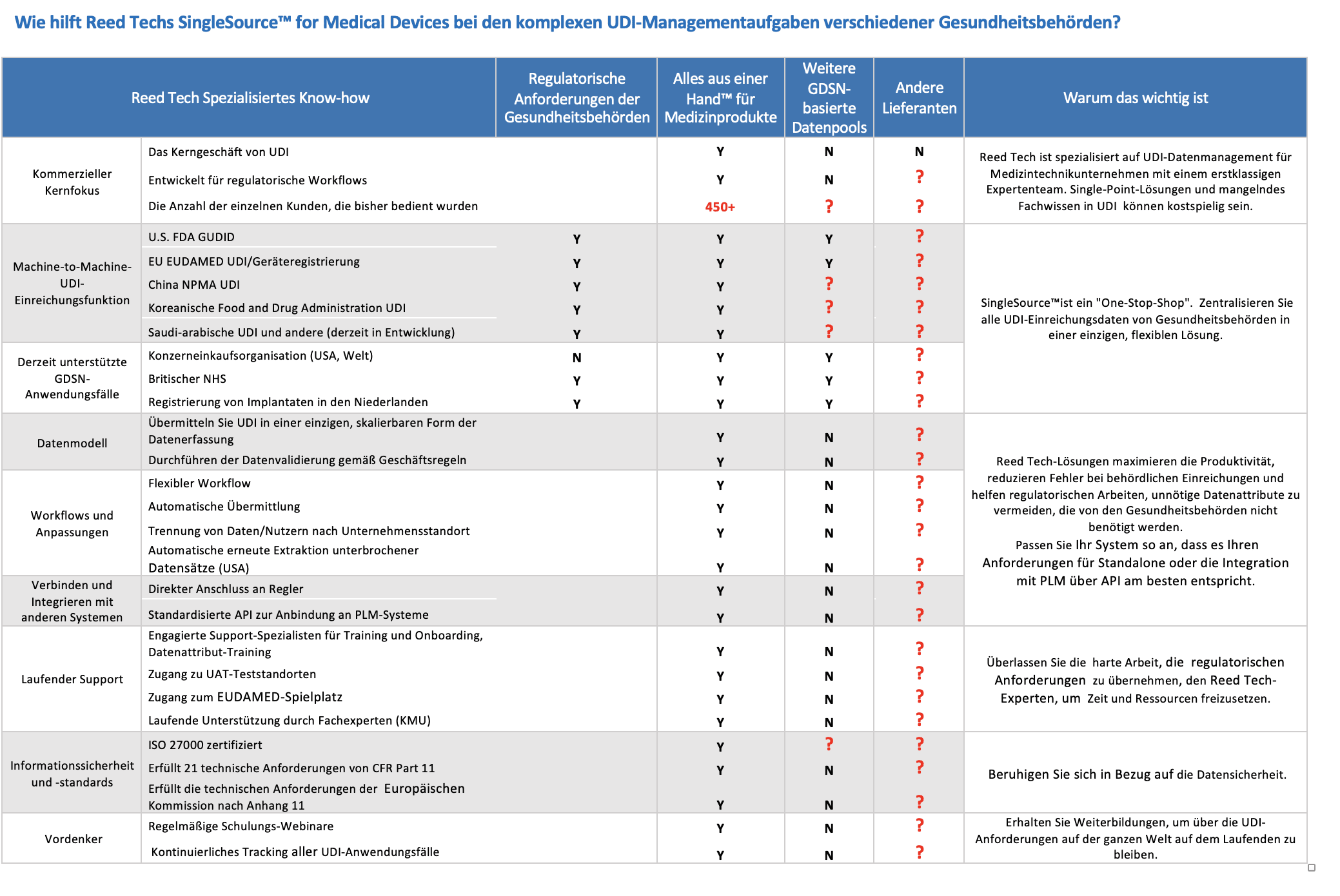
Wie kann Reed Tech SingleSource™ for Medical Devices helfen, die Komplexität von UDI für mehrere globale Gesundheitsbehörden zu bewältigen?
Beginnend mit der US-amerikanischen FDA führen Aufsichtsbehörden für Medizinprodukte in regionalen Märkten auf der ganzen Welt Konformitätsanforderungen zur eindeutigen Geräteidentifikation (UDI) ein. Zahlreiche Gesundheitsbehörden, darunter die Europäische Kommission, die chinesische NMPA, die südkoreanische MFDS und die niederländische LIR, haben Vorschriften erlassen, denen weitere folgen werden.
Medizingerätehersteller stellen fest, dass die UDI-Implementierung schwierig sein kann. Die Vorschriften sind neu, unterschiedlich klar und nicht harmonisiert. Sie haben unterschiedliche Gesetze, Richtlinien, Zeitpläne, Daten und Einreichungsansätze. Für Teams, die behördliche UDI-Daten verwalten, kann die Vorbereitung, Sammlung, Übermittlung und Pflege von Details schnell zu einer komplexen und mühsamen Aufgabe werden.
Aktivieren und bezahlen Sie Kanäle, wenn Sie in diesen Markt eintreten, was nicht in einem gebündelten Tarif enthalten ist.
Was kann Reed Tech SingleSource™ für medizinische Geräte für Ihr Team tun?
Die Herausforderung
Erzielen von Compliance – Wenden Sie sich für alle Kanäle der Gesundheitsbehörden mit regulatorischen Anforderungen an die UDI-Expertise mit einer einzigen, skalierbaren und flexiblen Lösung zum Sammeln, Pflegen, Validieren und Einreichen von Produktdaten.
Nutzung eines gesetzlichen Vertreters im Land – Weisen Sie Unternehmensbenutzern und lokalen Tochtergesellschaften Rollen/Verantwortlichkeiten zu, um eine gemeinsame Teamansicht der UDI-Daten zu erhalten. Vermeiden Sie Mehrfachkosten und sorgen Sie für Transparenz.
Maximierung der Bemühungen – Eine „Quelle der Wahrheit“ ist erforderlich, um die Kanäle der Gesundheitsbehörden einzuhalten und unterschiedliche Produktattribute, Datenvalidierungsregeln und Einreichungsstandards von Land zu Land vorwegzunehmen.
Gemeinsame Nutzung konsistenter Daten – Kommerzielle Handelspartner innerhalb der Lieferkette benötigen denselben Produktdatensatz, der für die behördliche Einreichung entweder über den globalen Datenpool oder auf andere Weise verwendet wird.
Vertrauenswürdiges Fachwissen – Der elektronische Einreichungsprozess und die Geschäftsregeln tragen von Region zu Region Nuancen.
Kostenvorhersehbarkeit – Schützen Sie Ihr Budget mit einer einzigen Lösung, wenn neue Regulierungsbehörden ins Spiel kommen. Stellen Sie sicher, dass die Geschäftskontinuität mit minimalen Unterbrechungen erreicht wird.
Fachliche Expertise – zu navigieren, zu verstehen und zu reagieren ist eine Notwendigkeit.
Funktionen von SingleSource™ für medizinische Geräte
Erfahren Sie mehr über Ansätze zur Verwaltung von UDI-Produktdaten
„Wir wurden Schritt für Schritt durch den Prozess geführt, und wenn wir auf ein Problem stießen, wurde es umgehend gelöst.“
-Operations Head für den Vertrieb von Medizinprodukten
SingleSource™ für Medizinprodukte
SingleSource™ for Medical Devices wurde entwickelt, um die Produktdatenverwaltungsanforderungen von Herstellern medizinischer Geräte zu erfüllen. Sehen Sie, was es für Sie tun kann.
Melden Sie sich noch heute für eine Demo an.
Über ReedTech
Reed Tech, ein Unternehmen von LexisNexis, kann Sie in Ihrer beruflichen Funktion mit Informationen über unsere anderen Produkte, Dienstleistungen und Veranstaltungen kontaktieren, von denen wir glauben, dass sie von Interesse sein könnten. Sie können Ihre Kommunikationspräferenzen jederzeit aktualisieren, indem Sie auf den in unseren Mitteilungen bereitgestellten Link zum Abbestellen klicken. Sie können mehr darüber erfahren, wie wir mit Ihren personenbezogenen Daten und Ihren Rechten umgehen, indem Sie unsere Datenschutzrichtlinie lesen.
EINREICHEN
Kontakt zu Reed Tech Life Sciences:
Mail: [email protected]
Telefon: +1-215-557-3010
Questions? We are here to help. Visit our Knowledge Center or Contact Us.