료기기 제품 데이터 관리
Reed Tech SingleSource™ for Medical Devices
여러 보건 당국의 복잡한 UDI 관리 작업에 Reed Tech사의 SingleSource™ for Medical Devices가 어떻게 도움을 줍니까
미국 FDA를 시작으로 의료 기기 규제 기관들은 전 세계 시장에서 UDI(고유 기기 식별) 규정 준수 요구 사항을 제정하고 있습니다. 유럽연합 집행위원회, 중국 NMPA, 한국 식품의약품안전처 및 네덜란드 LIR을 포함한 수많은 보건 당국은 규제를 강화하고 있습니다.
의료 기기 제조업체들은 UDI 구현이 어려울 수 있음을 알고 있습니다. 해당 규정들은 새롭고, 다양한 수준의 명확성을 가지고 있으며, 서로 일치하지 않습니다. 그들은 서로 다른 법률, 정책, 시기, 데이터 및 제출 방식을 가지고 있습니다. UDI 규제 데이터를 관리하는 팀에게 준비, 수집, 제출 및 유지 관련 세부 사항들은 복잡하고 부담스러운 작업이 될 수 있습니다.
번들된 전체 요금을 지불하는 대신, 각각의 시장에 진입할 때마다 채널을 활성화하고 비용을 지불하십시오.
Reed Tech SingleSource™ for Medical Devices가 귀하의 팀을 위해 무엇을 할 수 있습니까?
도전
(The Challenge)
규정 준수 (Compliance) 달성 – 규제 요구 사항이 있는 모든 보건 당국 채널에 제품 데이터 수집, 유지, 검증 및 제출을 위해 확장 가능하고 유연한 단일 솔루션과 함께 UDI 전문성을 갖추십시오.
국내 법률 대리인 활용 – UDI 데이터에 대한 팀 간의 공유를 위해 기업 사용자 및 계열사들에 역할 과 책임을 할당합니다. 중복된 비용 지출을 피하고 투명성을 제공합니다.
노력 극대화 – 국가별로 제품 속성, 데이터 검증 규칙 및 제출 표준이 다르므로, 보건 당국 규제를 준수하기 위해 하나의 ‘진실된 출처(Source of Truth)’가 필요합니다.
일관된 데이터 공유 – 공급망 내의 거래 파트너들은 글로벌 데이터 풀 또는 기타 수단을 통해 규제 제출에 사용되는 것과 동일한 제품 데이터를 필요로 합니다.
신뢰할 수 있는 전문성 – 전자 제출 프로세스 및 비즈니스 규칙은 지역마다 미묘한 차이를 가지고 있습니다.
비용 예측 가능성 – 새로운 규제가 도입될 때 단일 솔루션으로 귀사의 예산을 보호하십시오. 방해받지 않는 비즈니스 연속성을 보장합니다.
주제별 전문성 – 탐색하고 이해하고 대응하는 것은 필수입니다.
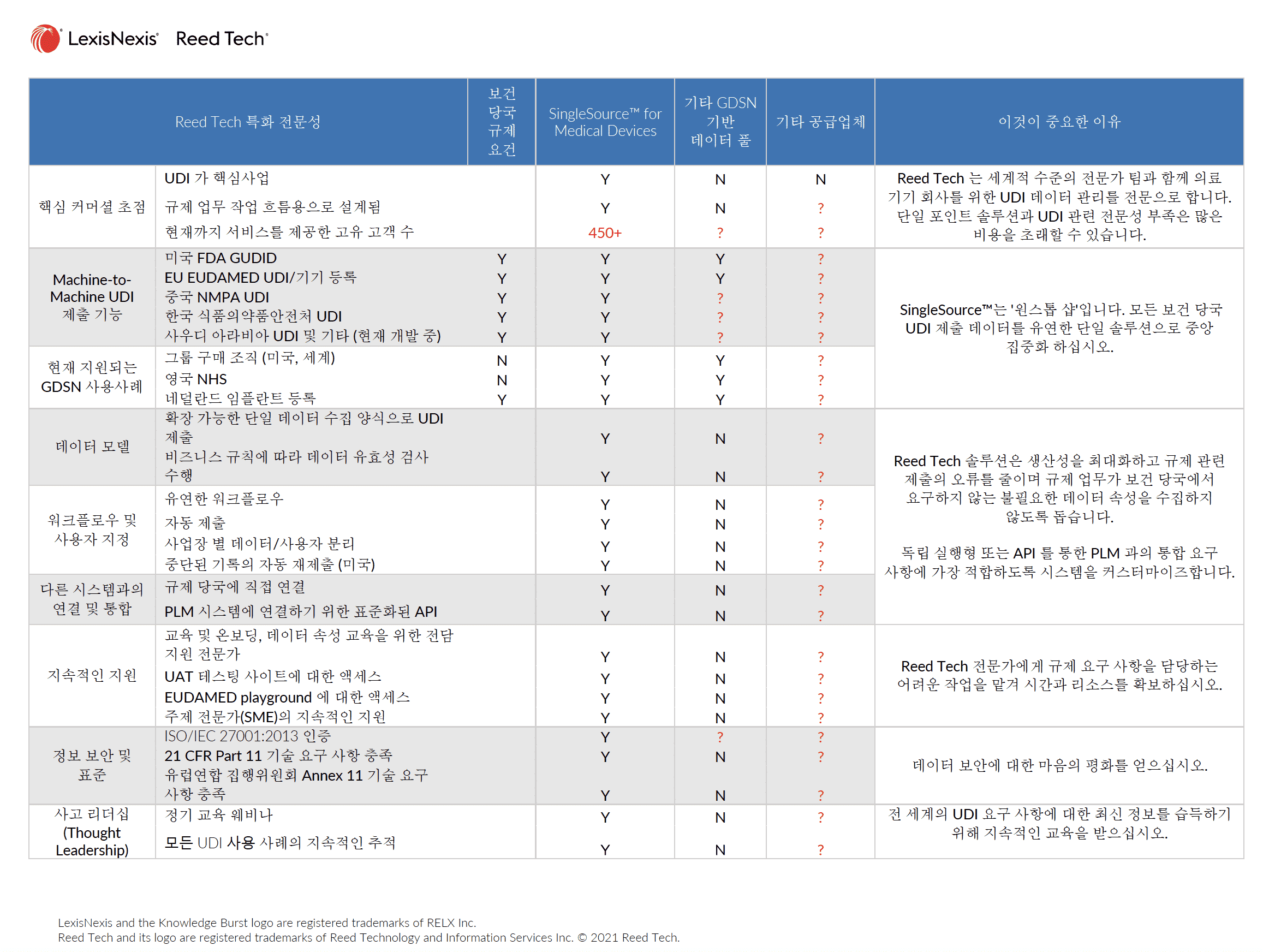
SingleSource™ for Medical Devices 의 특징
(Features)
“우리는 프로세스를 밟는 동안 단계별로 안내 받았고, 문제가 발견되면 즉시 해결되었습니다.”
-의료기기 공급업체의 운영 책임자
SingleSource™ for Medical Devices
SingleSource™ for Medical Devices 의료기기 제조업체의 제품 데이터 관리 요구 사항을 충족시키기 위해 만들어졌습니다. 그것이 귀하를 위해 뭘 해줄 수 있는지 보십시오.
지금 데모에 등록하십시오.
질문? 저희가 도와드리겠습니다. 지식 센터를 방문하거나 문의하십시오.